何娅 吴福蓉 崔振玲 (上海同济大学附属上海肺科医院 200433)
【摘要】 以2-巯基苯并咪唑为起始原料,经烷基化反应得到硫醚类化合物,得到的化合物进行了初步的体外抗结核杆菌H37Rv (M.tuberculosis,ATCC27294)活性测试,结果表明得到的部分硫醚化合物具有较好的体外抗结核活性.
【关键词】 苯并咪唑衍生物 合成 抗结核活性
【中图分类号】R914 【文献标识码】A 【文章编号】2095-1752(2013)32-0069-02
结核病(TB)是由结核分枝杆菌引起的慢性传染疾病,是人类的主要传染病之一。目前,全球的结核病呈上升趋势,每年新发病例约800万,死亡人数达200多万。由于耐药及多耐药菌株(Multi-Drug Resistant Tuberculosis MDR-TB)的出现,使得结核病的治疗难度加大,开发新的结核治疗药物已成为一项紧迫的任务。
硫醚类化合物具有许多重要的活性,如抗菌[1]、抗肿瘤[2]、抗病毒[3]、抗寄生虫[4]和抗雌激素受体[5]等多种生物活性,有研究显示此类化合物对多种结核杆菌具有显著地抑制活性[6],到目前为止,有关此类化合物对结核准株H37Rv的活性以及构效关系研究的报道还未见报道。有关此类化合物的生物活性引起了我们的研究兴趣,我们开展了有关此类化合物的深入研究,合成得到了苯并咪唑衍生物(图1),拟通过合成不同的苯并咪唑类硫醚和砜类化合物,考察不同链长以及苯环取代后对于活性的影响。我们的合成以2-巯基苯并咪唑1为起始原料,在甲醇溶液中,在甲醇钠作用下于室温条件下反应得到2,化合物2进行了初步的体外抗结核准株H37Rv活性测试。本文报道对这些硫醚类化合物的合成以及初步的抗结核活性研究结果。
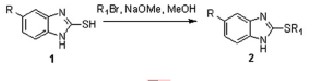 图 1
图 1
表 1合成的化合物2及抗结核杆菌H37Rv活性
RR1MIC
(μg/mL)RR1MIC
(μg/mL)
2aHEt1282bHBu128
2cHBn643dHp-NO2Bn32
2eMeEt642fMeBu32
2gMeBn322hMep-NO2Bn16
1 结果与讨论
1.1 目标化合物的合成
杂环硫醚类化合物的合成通常由巯基化合物和卤代物在K2CO3/醇体系中或在相转移催化剂催化下,在氢氧化钾、碳酸钾等水溶液和有机溶剂体系中反应制得[10],我们采用甲醇钠/甲醇体系中进行反应。甲醇钠使用量是本反应的关键,如果甲醇钠用量不足,会使反应不完全,如果甲醇钠用量太多,生成的副反应产物会增多,因而巯基化合物2与甲醇钠的摩尔比以1:1.2比较合适。
1.2 体外抗结核活性
实验结果如表1所示。从测试结果可以看出,硫醚类的苯并咪唑类化合物都具有一定的活性。苯环上被甲基取代后活性都得到增加。而不同的烷基取代对于活性有重要的影响,与乙基取代相比,由碳链较长的丁基、苄基的取代的后活性显著提高,最低抑制浓度MIC为16 μg/mL。结果也表明,当苄基对位被硝基取代后,活性也得到显著提高。 通过上述的研究表明一定长度的烷基链和链上取代可以提高抗结核杆菌活性。通过以上研究初步确立了此类化合物有关抗结核活性的构效关系。
尽管与商业化药物异烟肼(MIC=0.025μg/mL)相比,此类化合物的MIC还是偏高,但我们认为通过这样的结构改造得到的部分化合物对于抑制结核分支杆菌活性具有一定的功效,将为新型作用机制下的抗结核药物研发提供很好的思路,值得进一步研究与探讨,对于此类化合物进一步的抗结核活性以及构效关系研究还在进行中。
2 结论
本文通过合成得到的含巯基杂环类化合物与溴代物缩合,合成了一系列杂环硫醚类化合物, 得到化合物的结构经氢谱确证。通过体外抗结核活性的分析, 发现一些化合物具有一定的抗结核活性。本研究为此类化合物进一步的构效关系研究奠定了良好基础。
3 实验部分
3.1 仪器与试剂
核磁共振由Varian EM-360,EM-390型核磁共振仪,化学位移以氘代试剂中残留的质子信号为内标.比浊仪(美国Becton,Dickinson)、37℃培养箱(隔水式恒温培养箱,上海精宏实验设备有限公司)、细菌培养板即96孔U型板(浙江拱东医疗科技有限公司),快速柱层析采用青岛海洋化工厂或烟台化工研究所实验厂生产柱硅胶H(100~200,200~300目,10~40?mo/L),或者薄层层析硅胶H。结核分枝杆菌标准株H37Rv(M.tuberculosis,ATCC27294),来自国家菌种保存中心,液体培养基Middlebrook7H9培养基干粉和营养添加剂(OADC)购自美国BectonDickinson(BD)公司;应用液为含10%营养添加剂的Middlebrook7H9液体培养基。青霉素:注射用青霉素钠,华北制药股份有限公司,吐温购自美国sigma公司。
3.2 实验方法
3.2.1 化合物2的合成
在冰水浴冷却,氮气保护下,于5ml甲醇中,边搅拌边分批加入69mg金属钠,待气泡消失后,加入2mmol含巯基化合物2和3mmol溴代物,于室温搅拌过夜后加入15mL水,乙酸乙酯提取,饱和食盐水洗涤,硫酸镁干燥,过滤浓缩,残余物经柱层析得化合物3。
2-乙硫基苯并咪唑(2a): 白色固体, m.p.:171.8-173.0 ℃,收率76%. 1H NMR(CDCl3,300 MHz)δ:1.33(3H,t,J=7.2Hz),3.23(2H,q,J=7.2Hz),7.01–7.13(2H,m),7.33–7.51(2H,m)。
2-丁硫基苯并咪唑(2b): 白色固体, m.p.:132.1-133.3 ℃, 收率73%. 1H NMR (CDCl3,300 MHz)δ:0.89(3H,t,J=7.2Hz),1.33–1.52(2H,m),1.61–1.74(2H,m),3.26(2H,t,J=7.2Hz),7.05–7.15(2H,m),7.35–7.50(2H,m)。
2-苄基硫基苯并咪唑(2c):白色固体,m.p.:181.6-182.0℃,收率70%.1H NMR(CDCl3,300 MHz)δ:4.59(2H,s),7.01–7.13(2H,m),7.21–7.35(3H,m),7.42–7.52(4H,m)。
2-(4-硝基苄基)硫基苯并咪唑(2d):白色固体,m.p.:188.2-190.4℃,收率71%.1 HNMR(CDCl3,300 MHz)δ:4.69(2H,s),7.02–7.13(2H,m),7.33–7.57(2H,m),7.71–7.79(2H,m),8.09–8.20(2H,m)。
5-甲基-2-乙硫基苯并咪唑(2e):白色固体,m.p.130.5-132.5℃,收率86%.1H NMR(CDCl3,300 MHz)δ:1.39(t,J=7.5Hz,3H),2.43(s,3H),3.30(q,J=7.5Hz,2H),7.02(d,J=8.1Hz,1H),7.30(s,1H),7.42(d,J=8.1Hz,1H)。
5-甲基-2-丁硫基苯并咪唑(2f):白色固体,m.p.130.9-131.9℃,收率82%.1H NMR(CDCl3,300 MHz)δ:0.86(t,J=7.2Hz,3H),1.35~1.43(m,2H),1.66-1.73(m,2H),2.43(s,3H),3.30(t,J=7.5Hz,2H), 7.02 (d, J=8.4Hz,1H),7.31(s,1H),7.42(d,J=8.4Hz,1H)。
5-甲基-2-苄硫基苯并咪唑(2g):白色固体,m.p.143.5-146.0℃,收率80%.1H NMR(CDCl3,300 MHz)δ:2.43(s,3H),4.50(s,2H),7.02(d,J=8.4Hz,1H),7.27(s,1H),7.21~7.24(m,3H),7.29~7.31(m,2H),7.4,3(d,J=8.4Hz,1H)。
5-甲基-2-(4-硝基苄基)硫基苯并咪唑(2h):浅白色固体,m.p.170.5-172.5℃,收率73%.1H NMR(CD3OD,300 MHz)δ:2.40(s,3H),4.52(s,2H),7.02(d,J=8.4Hz,1H),7.24(s,1H),7.33(d,J=8.4Hz,1H),7.52(d,J=8.4Hz,2H),8.07(d,J=8.4Hz,2H)。
3.2.3 体外抗结核活性测试
将测试样品用DMSO溶解配制至1mg/mL,再用液体培养基将药物浓度从128μg/mL加倍稀释直至0.25μg/mL。在96孔细胞培养板外围孔中加生理盐水200μL以防止蒸发,其余每孔加10个浓度的含药培养基100μL,对照孔(每个浓度两副孔)加100μL无药培养基。37℃无菌试验24h后,加入含有Rv培养基(1mg/mL的Rv,配成终浓度2%),含药孔每孔加100μL。以异烟肼(INH)为质控内参,观察其活性。
记录结核菌生长孔中样品的最低浓度,即为样品最低抑制浓度(MIC)。MIC值测定重复3次,结果见表1。
参考文献
[1] (a) Bao, X.; Lin, X.; Jian, J.; Zhang, F.; Zou, L. Chin. J. Org. Chem. 2013, 33, 995 .
[2] Gong, J.; Sheng, L.; Yao, L.; Li, J.; Zhou, Y.; Guo, Y. Chin. J. Org. Chem. 2012, 32, 593.
[3] Gardiner, J. M.; Loyns, C. R.; Burke, A.; Khan, A.; Mahmood, N. Bioorg. Med. Chem. Lett. 1995, 5, 1307.
[4] Valdez, J.; Cedillo, R.; Hernández-Campos, A.; Yépez, L.; Hernández-Luis, F.; Navarrete-Vázquez, G.; Tapia, A.; Cortés, R.; Hernández, M.; Castillo, R. Bioorg. Med. Chem. Lett. 2002, 12, 2221.
[5] Munuganti, R. S. N.; Leblanc, Axerio-Cilies, P.; E.; Labriere, C.; Frewin, K.; Singh, K.; Hassona, M. D. H.; Lack, N. A.; Li, H.; Ban, F.; Guns, E. T.; Young, R.; Rennie, P. S.; Cherkasov, A. J. Med. Chem. 2013 56, 1136.
[6] Klime?ová, V.; Ko?í, J.; Pour, M.; Stachel, J.; Waisser, K.; Kaustova; J. Eur. J. Med. Chem. 2002, 37, 409.
[7] Kumar, R. V.; Gopal, K. R.; Kumar Seshu, K. V. S. R. J. Heterocyclic Chem. 2005, 42, 1405.
论文作者:何娅,吴福蓉,崔振玲
论文发表刊物:《医药前沿》2013年11月第32期供稿
论文发表时间:2014-1-3
标签:苯并咪唑论文; 活性论文; 化合物论文; 收率论文; 甲醇论文; 培养基论文; 抗结核论文; 《医药前沿》2013年11月第32期供稿论文;
